发稿时间:2022-10-31 来源: 药智网
2022年10月,全球多款创新疗法获批上市。美国FDA批准5款新药上市(NDA/BLA),包含2款抗体药物,3款改良型新药;NMPA批准华领医药首创新药多格列艾汀片上市,还有多款改良型新药、以及新适应症获得批准。
美国FDA批准的新药
FDA下属药品审评和研究中心(以下称CDER)在2022年10月批准了2款新药上市,分别为:
阿斯利康公司的Imjudo(通用名:tremelimumab),联合英飞凡(通用名:度伐利尤单抗)用于治疗不可切除的肝细胞癌 (HCC) 成年患者。
强生公司的Tecvayli(通用名:teclistamab),用于治疗复发/难治性多发性骨髓瘤。
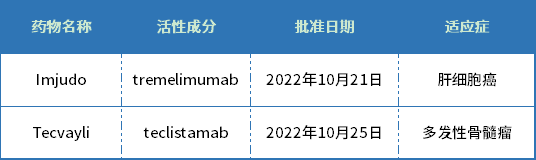
表1 2022年10月美国FDA批准的首创新药
Imjudo (tremelimumab)
Tremelimumab是阿斯利康开发的一种人源化的抗CTLA-4抗体,可以阻断CTLA-4、促进T细胞活化并加强对癌症的免疫反应。度伐利尤单抗是一种人源化的PD-L1单克隆抗体,能够阻断PD-L1与PD-1和CD80的结合,从而阻断肿瘤免疫逃逸并解除对免疫反应的抑制。
Tremelimumab+度伐利尤单抗联合方案也被称之为STRIDE方案,曾获FDA授予的优先审评资格。本次批准是基于Ⅲ期临床研究HIMALAYA的阳性结果。在该研究中,与索拉非尼单药治疗相比,接受tremelimumab联合度伐利尤单抗治疗的患者死亡风险降低了22% 。《新英格兰医学证据杂志》上发表的这一结果显示约有31%接受联合治疗的患者在三年后仍然存活,而接受索拉非尼单药治疗的患者中仅有20%在相同的随访期间内仍然存活。
Tecvayli (teclistamab)
Teclistamab是强生公司开发的一款BCMA/CD3双抗,用于治疗复发/难治性多发性骨髓瘤。这是首款获批治疗多发性骨髓瘤的双特异性疗法,也是首款获批靶向BCMA的双特异性抗体,今年8月已率先在欧盟获批上市,在中国已于去年6月获批临床。
此次BLA是基于MajesTEC-1研究(NCT04557098,NCT03145181)的结果。该研究入组的是先前已接受过多种方案治疗的复发或难治性多发性骨髓瘤(R/R MM)患者,结果显示,teclistamab治疗的总缓解率(ORR)为61.8%,CR为28.2%。首次响应的平均时间为1.2个月,6个月时DOR率为90.6%,9个月时DOR率为66.5%。所有患者都经过蛋白酶体抑制剂、免疫抑制剂、CD38抗体治疗,其中76%的患者经过这种治疗后复发。
除了原创新药,10月FDA还批准了3款改良型新药,包括头孢唑林钠散剂、 呋塞米皮下注射剂、重酒石酸去甲肾上腺素溶液剂。
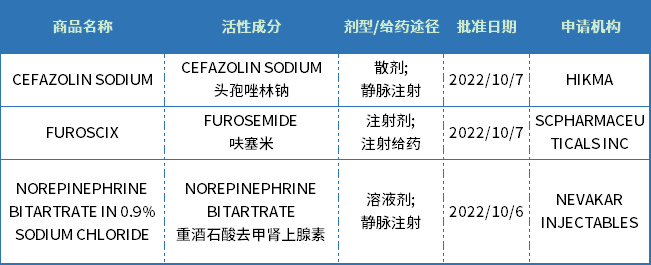
表2 2022年10月美国FDA批准的改良型新药
NMPA批准的新药
2022年10月,中国国家药品监督管理局(NMPA)共批准了9款新药,包括1款1类创新药,5款2类新药,以及3款生物制品。

表3 2022年10月NMPA批准的国产新药
多格列艾汀片
多格列艾汀片(dorzagliatin,商品名:华堂宁)是华领医药开发的一款1类创新药,是葡萄糖激酶(GK)激活剂,作用于胰岛、肠道内分泌细胞以及肝脏等葡萄糖储存与输出器官中的葡萄糖激酶靶点,适用于改善成人2型糖尿病患者的血糖控制。值得一提的是,2020年8月,华领医药与拜耳达成合作,拜耳获得该产品在中国独家商业化的权利,华领医药将获得3亿元人民币的预付款,此外其还将获得额外最高可达到41.8亿元人民币的里程碑付款。
注射用左亚叶酸钠
注射用左亚叶酸钠是南京海纳制药开发的一款2.2类新药。左亚叶酸是亚叶酸的活性成分,是多种癌症联合化疗药物中使用最广泛的化疗辅助药物。目前中国已有多家公司的注射用左亚叶酸钙获批上市,而注射用左亚叶酸钠是一种新剂型,目前仅汇伦医药和南京海纳制药两家获批。
兰索拉唑碳酸氢钠胶囊
兰索拉唑碳酸氢钠胶囊是北京四环制药开发的一款2.2类新药,是一款质子泵抑制剂复方制剂,成分中抗酸药(碳酸氢钠)可直接中和胃酸,使兰索拉唑在吸收前不被胃酸分解,从而达到持久抑制胃酸的效果。厦门恩成制药的兰索拉唑碳酸氢钠胶囊也已申报上市。
艾司奥美拉唑镁碳酸氢钠胶囊
艾司奥美拉唑镁碳酸氢钠胶囊是长春海悦药业开发的一款2.3类新药,也是质子泵抑制剂复方制剂,用于治疗胃食管反流病,与适当的抗菌疗法联合用药根除幽门螺杆菌。
妥布霉素吸入溶液
妥布霉素是一种临床耐药性较少的氨基糖苷类抗生素,是用作肺部铜绿假单胞菌早期感染的一线治疗药物。妥布霉素吸入溶液最早由 PathoGenesis 公司(2001 年被 Novartis 收购)开发,于1997 年12 月被FDA 批准上市。健康元的妥布霉素吸入溶液是针对我国支气管扩张症的高发病率和临床药物匮乏的现状而研制出来的抗菌药物新型吸入制剂,是国内首款获批上市的吸入抗生素类药物。
环泊酚注射液
环泊酚注射液(HSK3486乳状注射液)是海思科研发的一款全新具有自主知识产权的静脉麻醉药物,其活性成分环泊酚是(R)-构型异构体小分子药物,为GABAA受体激动剂。2020年12月,环泊酚注射液首次在中国获批,用于消化道内镜检查中的镇静,此后又相继获批用于全身麻醉诱导、支气管镜检查中的镇静、全身麻醉诱导和维持、重症监护期间的镇静,本次获批新适应症:妇科门诊手术的镇静及麻醉。
此外,北京北生研生物制品有限公司的ACYW135群脑膜炎球菌多糖疫苗、宜昌东阳光长江药业的门冬胰岛素注射液获批上市,药明巨诺的瑞基奥仑赛注射液获批新适应症:用于治疗经过二线或以上系统性治疗的成人难治性或24个月内复发的滤泡性淋巴瘤(r/rFL)。
除了国产创新药,NMPA在本月还批准了多款进口新药,详情见下表:
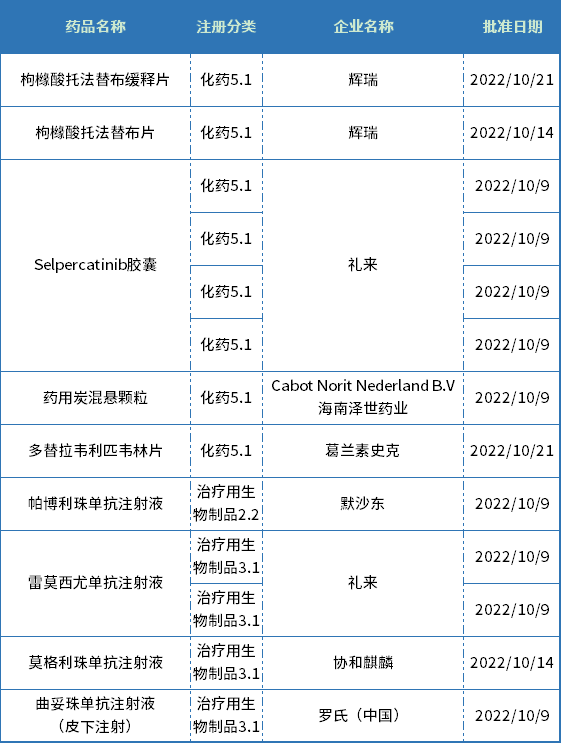
表4 2022年10月NMPA批准的进口新药
这些进口新药适应症主要集中在自身免疫性疾病、肿瘤及抗病毒领域,来自辉瑞、礼来、葛兰素史克、默沙东、罗氏、协和麒麟等跨国药企。
